





 Рейтинг: 4.2/5.0 (1917 проголосовавших)
Рейтинг: 4.2/5.0 (1917 проголосовавших)Категория: Инструкции
Разработка инструкции по радиационной стерилизации
- Стерилизация – важный этап в производстве медицинских изделий. Процесс радиационной стерилизации связан с облучением изделия ионизирующим излучением. При правильном проведении радиационная стерилизация является безопасным и надежным промышленным процессом.
- Обоснование применения стерилизующей и максимально допускаемой дозы облучения основывается на требованиях стандартов ГОСТ Р ИСО 11137 «Стерилизация медицинской продукции. Радиационная стерилизация» и ГОСТ Р ИСО 11737 «Стерилизация медицинских изделий. Микробиологические методы».
- Отступление от правил проведения процесса стерилизации или неадекватное применение диапазона доз ионизирующего излучения может привести к ухудшению свойств медицинского изделия. Под действием высоких доз радиации происходит деградация полимерного материала, растрескивание, нарушение герметичности упаковки и т.п. Медицинское изделие может нести опасность для здоровья человека.
- Оценку пригодности продукции для использования по назначению после радиационной стерилизации проводят по основополагающими стандартам серии ГОСТ Р ИСО 10993 «Изделия медицинские. Оценка биологического действия медицинских изделий».
АНО «ИМБИИТ»
Адрес: 123557, г. Москва, Большой Тишинский пер. д. 43/20, стр. 2.
карта проезда:
Контакты: Факс/тел. 8 (499) 252-24-22, мобильный +7 926 538 90 83
Заявки на проведение работ направлять на адрес электронной почты: zakaz@imbiit.com
7,1. Подготовка изделий медицинского назначения (далее- изделия) к применению включает три этапа: дезинфекцию, предстерилизационную очистку, стерилизацию.
7,2. Дезинфекцию изделий проводят с целью уничтожения вегетативных форм патогенных и условно – патогенных микроорганизмов – вирусов ( в том числе возбудителей парентеральных вирусных гепатитов, ВИЧ – инфекции), бактерий,( включая микобактерии туберкулёза), грибов (включая грибы рода Кандида) на ИМН, а также в их каналах и полостях.
7,3.Предстерилизационную очистку ИМН проводят с целью удаления с них белковых, жировых и механических загрязнений, а также остатков лекарственных препаратов.
7,4. Стерилизацию проводят с целью уничтожения всех патогенных и непатогенных микроорганизмов, включая их споровые формы.
7,5. Дезинфекцию, предстерилизационную очистку и стерилизацию изделий осуществляют в соответствии с требованиями действующих руководящих и нормативно – методических документов (ОСТ 42-21-2-85 «Стерилизация и дезинфекция ИМН. Методы, средства, режимы»; Методические указания по дезинфекции, предстерилизационной очистке и стерилизации ИМН» от 30,12,98. №МУ – 287-113 и др).
7,6. При использовании средств, обладающих одновременно дезинфецирующими и моющими свойствами, дезинфекция изделий может быть совмещена с их предстерилизационной очисткой в одном процессе.
7,7. Дезинфекция ИМН.
7,7,1.Дезинфекция ИМН направлена на профилактику внутрибольничного инфицирования пациентов и медицинских работников.
7,7,2. Дезинфекции подлежат все ИМН после контакта с пациентом.
7,7,3. Дезинфекцию ИМН осуществляют непосредственно в отделениях - физическим (кипячение, паровой, воздушный) и химическим ( растворами химических средств) методами.
7,7,4. Дезинфекция с использованием химических средств производится способом погружения изделия в раствор дезинфектанта в специальных ёмкостях из стекла, пластмасс, или покрытых эмалью без повреждений. Ёмкости должны быть снабжены крышками, потопителями, иметь чёткие надписи с указанием названия средства, его концентрации, назначения, даты приготовления.
7,7,5. После дезинфекции ИМН тщательно промываются в проточной воде, после чего высушиваются, упаковываются и направляются для стерилизации.
7,8. Предстерилизационная очистка ИМН.
7,8,1.Предстеридизационной очистке подвергаются ИМН многократного применения, подлежащие стерилизации. Предстерилизационную очистку проводят механизированным или ручным способом.
7,8,2. При наличии у средства наряду с моющими также и антимикробных свойств, предстерилизационная очистка может быть совмещена с их дезинфекцией.
7,8,3. Контроль качества предстерилизационной очистки в отделениях проводится в порядке самоконтроля ежедневно. Контролю подвергают 1% одновременно обработанных изделий каждого наименования, но не менее трёх единиц.
7,8,4. Качество очистки ИМН проверяется путём постановки Азопирамовой пробы на наличие остаточных количеств крови, а также Фенолфталеиновой пробы на наличие остаточных количеств щелочных компонентов, моющих средств. В случае положительной пробы на кровь или щелочные компоненты моющих средств всю партию изделия. из которых отбирали контроль, подвергают повторной очистке до получения отрицательных результатов.
7,8,5. Результаты контроля отражают в специальном журнале. ( Журнал учёта качества предстерилизационной обработки).
7,9. Стерилизация ИМН.
7,9,1.Стерилизации подвергаются все изделия, соприкасающиеся с раневой поверхностью, контактирующие с кровью, другими биологическими жидкостями пациента и инъекционными препаратами. А также изделия, которые в процессе лечебно – диагностического процесса соприкасались со слизистой оболочкой и могут вызвать её повреждение.
7,9,10. Стерилизацию осуществляют физическими (паровой, воздушный), химическими ( применение растворов химических средств) и газовым методами.
7,9,11. При паровом, воздушном, газовом методах изделия стерилизуют в упакованном виде, используя упаковочные материалы ( бумажные, пластиковые материалы, пергамент, бязь), используют, как правило однократно.
При паровом методе используют стерилизационные коробки (биксы) с фильтрами и без фильтра.
7,9,12. Паровым методом стерилизуют общие хирургические и специальные инструменты, хирургическое бельё, перевязочный материал, изделия из резин (перчатки, трубки, катетеры, зонды). Используется насыщенный пар под избыточным давлением. Температура 110-135 гр С.
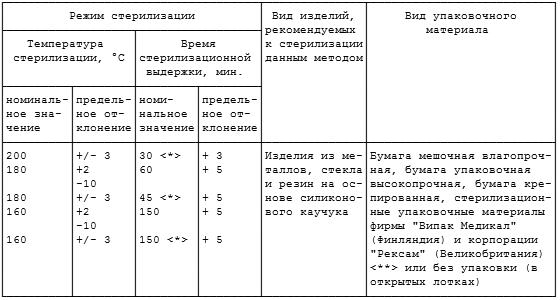
7,9,13.Воздушным методом стерилизуют хирургические, гинекологические, стоматологические инструменты. Перед стерилизацией инструменты обязательно высушивают в сухожаровом шкафу при температуре 85 г С до исчезновения видимой влаги. При воздушном методе стерилизующим средством является сухой горячий воздух с температурой 160-180 градусов С. При этом объекты стерилизации могут быть завёрнуты в крафт – пакеты, крепированную бумагу или стерилизоваться без упаковки, в открытых лотках, но тогда сразу используются по назначению. Время стерилизации: при температуре 180гр С – 60минут, при температуре 160гр С – 150 минут.
Сроки годности стерильности не вскрытых биксов: с фильтрами до 30 суток. Простые биксы до 3х суток. Крафт-пакеты до 20 дней. В бумаге или тканевой бязе - 3суток.
7,9,14. Химический метод стерилизации, применяют как правило только для термолабильных материалов. Используют специальные ёмкости с крышкой. Во избежание разбавления рабочих растворов, особенно используемых многократно, погружаемые в них изделия не должны содержать видимой влаги. После стерилизации все манипуляции проводят, строго соблюдая все правила асептики. Изделия промывают все стерильной жидкостью (питьевая вода, 0,9% раствор Натрия Хлорида), налитой в стерильные ёмкости. Промытые стерильные изделия используют сразу по назначению или помещают на хранение в стерильный бикс, выложенную стерильной простынёй, на срок не более 3 суток.
7,9,15. Контроль качества стерилизации в паровых и воздушных стерилизаторах контролируется с помощью индикаторов СТЕРИКОНТ, Количество индикаторов закладываемых в стерилизатор, зависит от объёма камеры. До 80 литров 5шт. Свыше 80 литров-однеокамерные 15. Пользоваться согласно инструкции. От листа с индикаторами отрывают необходимое количество индикаторов и нумеруют их. ( ПОКАЗАТЬ НА РИСУНКЕ) Индикаторв приклеивают цветовыми метками с внешней стороны упаковок. На бикс - к бирке на бумажную или плёночную упаковку. Индикаторы СТЕРИКОНТ не допускается размещать внутри стерилизуемых изделий. Для этого используют только индикаторы СТЕРИТЕСТ – В.
Бактериологический контроль за качеством стерилизации с помощью биотестов, проводится в плановом порядке не реже 2х раз в год.
Результаты контроля работы паровых и воздушных стерилизаторов заносятся в журнал «Учёта результатов контроля работы паровых и воздушных стерилизаторов».
7,10. Порядок проведения стерилизации в воздушном стерилизаторе.
7,10,1. Медицинские инструменты стерилизуются в открытом виде на расстоянии 2-3 см друг от друга в один ряд. В зависимости от объёма камеры, раскладываются индикаторные наклейки СТЕРИКОНТ в 5-15 точках. ( по инструкции СТЕРИКОНТа).
7,10,2. Делается запись в журнале стерилизации: вид инструментария и его количество; Время, когда температура внутри шкафа достигла заданной – 180гр или 160 гр ( начало), и время отключения ( конец).
7,10,3. После проведённого цикла стерилизации перед открытием сухожарового шкафа его ручка протирается дезинфицирующим раствором.
7,10,4. Открывается шкаф, когда температура в камере снизится до 50гр.
7,10,5. Термоиндикаторы сравниваются с эталонами: после чего они приклеиваются в графе «химический контроль», журнала учёта качества работы паровых и воздушных стерилизаторов.
1.1. Дезинфекция, предстерилизационная очистка и стерилизация изделий медицинского назначения (далее изделия) производятся с целью профилактики внутрибольничных инфекций у пациентов и персонала лечебно-профилактических учреждений (ЛПУ).
1.2. Дезинфекцию изделий (на поверхностях, а также в их каналах и полостях) проводят с целью уничтожения патогенных и условно-патогенных микроорганизмов: вирусов (в том числе возбудителей парентеральных вирусных гепатитов, ВИЧ-инфекции), вегетативных бактерий (включая микобактерии туберкулеза), грибов (включая грибы рода Кандида).
Дезинфекции подлежат все изделия после применения их у пациентов. После дезинфекции изделия промывают водопроводной водой, высушивают и применяют по назначению или (при наличии показаний) подвергают предстерилизационной очистке и стерилизации.
1.3. Стерилизацию изделий проводят с целью уничтожения микроорганизмов всех видов, в том числе споровых форм. Стерилизации подлежат все изделия, соприкасающиеся с раневой поверхностью, контактирующие с кровью в организме пациента или вводимой в него, инъекционными препаратами, а также изделия, которые в процессе эксплуатации контактируют со слизистой оболочкой и могут вызвать ее повреждение.
1.4. Изделия многократного применения, подлежащие стерилизации, перед стерилизацией подвергаются предстерилизационной очистке (ПСО). Предстерилизационную очистку проводят с целью удаления с изделий белковых, жировых и механических загрязнений, а также остатков лекарственных препаратов.
1.5. В качестве средств дезинфекции, предстерилизационной очистки и стерилизации в Республике Беларусь используются только разрешенные в установленном порядке физические и химические средства.
1.6. При выборе средств следует учитывать рекомендации изготовителей изделий, касающиеся воздействия конкретных средств на материалы этих изделий (из числа разрешенных в республике для данной цели).
При проведении дезинфекции, предстерилизационной очистки и стерилизации допускается использование оборудования (установки, моечные машины, стерилизаторы и др.), разрешенного в установленном порядке к промышленному выпуску и применению (в случае импортного оборудования - разрешенного к применению) в Республике Беларусь.
1.7. Емкости с растворами дезинфицирующих, моющих и стерилизующих средств должны быть изготовлены из коррозионностойких материалов, снабжены перфорированными поддонами и плотно закрывающимися крышками, иметь четкие надписи с указанием названия средства, его концентрации, даты приготовления (для готовых к применению средств, разрешенных для многократного использования, указывают дату начала использования средства).
1.8. Рекомендации по дезинфекции, предстерилизационной очистке и стерилизации сложных по конструкции изделии (эндоскопы, медицинские инструменты к гибким эндоскопам и др.), а также дополнительные сведения, касающиеся различных аспектов указанных видов обработки изделий, более подробно изложены в официальных инструктивно-методических документах.
Для стерилизации медицинских изделий мы стали применять бумажные пакеты для паровой и воздушнойстерилизации "Стериcепт ".
Мы использовали пакеты "Стериcепт" во всех режимахпаровой и воздушной стерилизации. Отметим, что довольны качеством продукции.
Стерилизационные пакеты "Стериcепт" полностью аналогичны пакетам для паровой и воздушнойстерилизации импортного производства.
Пакеты "Стериcепт" российского производства дешевле импортных аналогов. Это позволило нам уменьшить расходы на упаковку для стерилизации. улучшить качество стерилизации. бесперебойно получать упаковку для стерилизации "Стериcепт" любыми партиями и необходимых нам размеров.
Внедрение в нашу практику использование пакетов "Стериcепт" для паровой и воздушнойстерилизации позволило применять их в качестве групповой и транспортной упаковки.
Дезинфекция изделий медицинского назначения


Дезинфекция изделий медицинского назначения проводится с целью уничтожения патогенных и условно-патогенных микроорганизмов - вирусов (в т.ч. возбудителей парентеральных вирусных гепатитов, ВИЧ-инфекции), бактерий (включая микобактерии туберкулеза), грибов на изделиях медицинского назначения. а также в их каналах и полостях. Дезинфекции подлежат все изделия после применения их у пациента.
Дезинфекция. предстерилизационная очистка,стерилизация изделий медицинского назначения и контроль направлена на профилактику внутрибольничных инфекций у пациентов и персонала лечебно-профилактических учреждений.
Основные этапы обработки инструментов медицинского назначения:
I этап: дезинфекция
II этап: предстерилизационная очистка
III этап: стерилизация.
Дезинфекцию изделий осуществляют физическим и химическим методами. Выбор методадезинфекции зависит от особенностей изделия и его назначения.
Физический метод дезинфекции
кипячение
водяной насыщенный пар под давлением
сухой, горячий воздух
надежен, экологически чист и безопасен для персонала, поэтому в тех случаях, когда позволяют условия (оборудование, номенклатура изделий и т.д.), при проведении дезинфекции изделий предпочтение следует отдать этому методу.
Основные правила дезинфекции физическим методом.
1. Перед кипячением изделия очищают от органических загрязнений, промывая водопроводной водой с соблюдением мер противоэпидемической защиты. Отсчет времени дезинфекционной выдержки начинают с момента закипания воды.
2. При паровом методе предварительная очистка изделий не требуется. Их складывают в стерилизационные коробки и помещают в паровой стерилизатор.
3. Дезинфекцию воздушным методом проводят без упаковки в воздушном стерилизаторе. Этим методом можно дезинфицировать только изделия, не загрязненные органическими веществами.
Основные правила этапа дезинфекциимедицинского инструментария с использованием дезинфектантов.
1. в качестве средств стерилизации используют только разрешенные физические и химические средства (в настоящее время - 57 наименований).
2. при выборе средств следует учитывать рекомендации изготовителей изделий, касающиеся воздействия конкретных средств (из числа разрешенных в нашей стране для этой цели) на материалы этих изделий.
При проведении дезинфекции допускается использование только того оборудования, которое разрешено в установленном порядке к промышленному выпуску и применению.
3. Дезинфекцию с использованием химических средств проводят способом погружения изделий в раствор в специальных емкостях из стекла, пластмасс или покрытых эмалью БЕЗ ПОВРЕЖДЕНИЙ. Наиболее удобно применение специальных контейнеров, в которых изделия размещают на специальных перфорированных решетках. Емкости с растворами дезинфицирующих средств должны быть снабжены крышками, иметь четкие надписи с указанием названия средства, его концентрации и т.д.
4. Промывка изделий под проточной водой до дезинфекции НЕ ДОПУСКАЕТСЯ, т.к. аэрозоль, образующийся в процессе мытья, может инфицировать лиц, занимающихся обработкой, а также поверхности помещений.
Однако при применении многих альдегидосодержащих дезинфектантов очистка медицинских изделий от загрязнения является обязательной, так как эти дезинфектанты фиксируют белковые загрязнения, что затрудняет процесс дезинфекции. Такая очистка должна проводиться с соблюдением противоэпидемических принципов, в специальной емкости; промывные воды, салфетки, использованные для очистки, обеззараживаются одним из хлорсодержащих дезинфектантов.
5. Медизделия погружаются в дезраствор сразу же после применения таким образом, чтобы дезраствор полностью покрывал инструменты. Изделия сложной конфигурации дезинфицируют в разобранном виде. Каналы и полости изделий заполняют дезинфицирующим раствором так, чтобы в них не содержалось пузырьков воздуха.
6. Значительно загрязненные инструменты подвергают предварительной, а затем собственно дезинфекции.
7. Хлорсодержащие средства применяют в основном для дезинфекции изделий медицинского назначения из стекла, пластмассы, резины, коррозионно-стойкого материала (хлорамин Б, «Клорсепт» и др.)
8. По окончании дезинфекционной выдержки изделия промывают. Оставшиеся загрязнения тщательно отмывают с помощью механических средств (ерши, щетки, салфетки марлевые или бязевые и др.) проточной питьевой водой.
9. Ершевание резиновых изделий не допускается.
Стандарт дезинфекции шприцев однократного применения.
Для дезинфекции выделяются емкости с дезинфицирующим средством.
Первая емкость - для промывания.
Промывание проводится путем двух-трехкратного пропускания дезинфицирующего раствора через канал иглы и внутренней части шприца. Промывание заканчивается на пустом шприце. Не должно быть видимых остатков крови. Иглу не снимать!
Смена раствора производится по мере загрязнения. По не более 15 шприцев 0,5л. Возможен вариант набора дезинфицирующего средства в шприц и слив; пустую емкость, т.е. емкостей будет три.
Для дезинфекции инструментов однократного применения рекомендуется использовать хлорсодержащие средства.
При выполнении манипуляций на дому (участковая служба, скорая помоги медицинский работник должен иметь емкость с дезраствором для ополаскивания на месте. Затем шприцы складывают в плотно закрывающийся контейнер.
Основную дезинфекцию проводить в условиях медицинского учреждения.
Вторая емкость - «для дезинфекции ».
Емкость должна быть со «Съемным ситом». Дезинфицирующее средство набирается в шприц и вынимается поршень. Шприц дезинфицируется с иглой. Выдерживается время экспозиции согласно «Методическим рекомендациям».
Уничтожение острых предметов
1. чтобы избежать случайных уколов иглами, не сгибайте и не ломайте их перед уничтожением.
2. обеззараженные иглы должны быть помешены в непрокалываемый контейнер. Расположите контейнер близко к месту, где им будут пользоваться, чтобы не было необходимости переносить острые предметы перед выбрасыванием
3. выбросите герметично закрытый контейнер в мусоросборник
4. деформирование проводится в воздушном стерилизаторе при температуре 180 °С в течение 30 минут.
Как надевать колпачок на уже использованную иглу?
Всегда надевайте колпачок на иглу одной рукой, делая это следующим образом:
1. введите кончик иглы в колпачок
2. наклоните шприц так, чтобы колпачок сел на иглу.
3. другой рукой плотно наденьте колпачок на иглу.
Действуя подобным образом, вы предохраните себя и других от укола иглой.
Аккуратно обращайтесь с острым инструментарием - перчатки не предохраняют от повреждения кожи, но они частично очистят иглу от крови, уменьшая количество инокулянта.
Стандарт дезинфекция изделий медицинского назначения многократного применения.
Предстерилизационная очистка предусматривает окончательное удаление остатков белковых, жировых, механических загрязнений и остаточных количеств лекарственных препаратов.
Предстерилизационной очистке должны подвергаться все изделия, подлежащие стерилизации. Для этого этапа обработки изделий также используют только разрешенные моющие средства.
Разобранные изделия подвергают предстерилизационной очистке в разобранном виде с полным погружением и заполнением каналов. Мойку каждого изделия по окончании экспозиции проводят при помощи ерша, ватно-марлевого тампона и других приспособлений, необходимых при ручной очистке. Каналы изделий промывают с помощью шприца. Ершевание резиновых изделий не допускается. Предстерилизационную очистку ручным способом осуществляют в емкостях из пластмасс, стекла или покрытых эмалью (без повреждений).
Машинная мойка изделий предпочтительнее ручной вследствие ограничения контакта персонала с инфицированным материалом и возможности обеспечения более качественной очистки.
В настоящее время существует ряд средств, позволяющих объединить в один этап обработки дезинфекцию и предстерилизационную очистку.
Этапы дезинфекции. как и для одноразовых шприцев.
Рекомендуется использовать альдегидсодержащие средства, окислители, ЧАС.
Этапы предстерилизационной очистки
1 этап: промывание проточной водой после дезинфекции над раковиной в течение 30 секунд до полного уничтожения запаха дезсредств;
2 этап замачивание в моющем растворе при температуре воды 50°С на 15 минут шприцев и головок в разобранном состоянии;
3 этап: мытье каждого изделия в этом же растворе, где проводилось замачивание, с помощью ерша или ватного тампона в течение 30 секунд;
4 этап: споласкивание проточной водой (после моющего средства «Биолот» - 3 минуты; после растворов перекиси водорода с моющим средством «Прогресс» - 5 минут; после моющих средств «Астра», «Лотос» -10 минут);
5 этап: споласкивание дистиллированной водой в течение 30 секунд;
6 этап: просушивание горячим воздухом при температуре +75..+87 в сушильных шкафах.
От полноты и качества проведения предстерилизационной обработки впрямую зависит эффективность последующей стерилизации. поэтому нормативами в практику введен обязательный контроль качества предстерилизационной очистки. осуществляемой как самим лечебно-профилактическим учреждением, так и специалистами Госсанэпиднадзора, дезстанций.
Самоконтроль качества ПСО в отделениях лечебно-профилактических учреждений проводится ежедневно.
Организуется и контролируется старшей медсестрой не реже 1 раза в неделю.
В ЦСО - ежедневно!
Контролю подвергается 1% от одновременно отработанных изделий одного наименования, но не менее 3-5 единиц.
Контроль качества предстерилизационной очистки
Качество предстерилизационной очистки контролируют, определяя:
- кровь - с помощью азопирамивой пробы;
- масляные лекарственные загрязнения - с помощью пробы с суданом - 3;
- остатки моющих средств — с помощью фенолфталеиновой пробы.
При положительной пробе на кровь, моющее средство всюгруппу контролируемых изделий, от которой отбиралсяконтроль, подвергают повторной обработке до полученияотрицательных результатов.
28. Медицинское оборудование и изделия медицинского назначения (далее – ИМН) по степени контакта с организмом человека и риска инфицирования пациента подразделяются на три группы:
1) критические ИМН – инструменты и оборудование, непосредственно контактирующие с тканями, полостями или кровеносным руслом человека;
2) полукритические ИМН – инструменты и оборудование, контактирующие с неповрежденными слизистыми оболочками;
3) некритические ИМН – инструменты, оборудование и предметы ухода, контактирующие с интактным кожным покровом.
Критические ИМН подвергаются обязательной стерилизации, полукритические – дезинфекции высокого и среднего уровней, некритические – дезинфекции среднего и низкого уровней.
29. Дезинфекция и предстерилизационная очистка ИМН проводятся согласно приложениям 4, 5 к настоящим Санитарным правилам.
30. В организациях здравоохранения используется шовный материал, выпускаемый в стерильном виде. Категорически запрещено обрабатывать и хранить шовный материал в этиловом спирте.
31. При подготовке к использованию наркозно-дыхательной аппаратуры используют специальные бактериальные фильтры, предназначенные для оснащения указанной аппаратуры. Установку и замену фильтров осуществляют в соответствии с инструкцией по применению конкретного фильтра. Для заполнения резервуаров увлажнителей используется стерильная дистиллированная вода. Съемные детали аппаратов дезинфицируют так же, как ИМН из соответствующих материалов.
32. Предметы ухода за пациентами дезинфицируют следующими способами:
1) подкладные клеенки, фартуки, чехлы матрасов из полимерной пленки и клеенки - способом протирания тканевой салфеткой, смоченной раствором дезсредства;
2) кислородные маски, рожки от кислородной подушки, шланги электро/вакуум отсосов, медицинские термометры, судна, мочеприемники, тазики эмалированные, наконечники для клизм, резиновые клизмы – способом погружения в раствор дезсредства с последующим промыванием водой;
3) для обработки предметов ухода (без их маркировки) за пациентами возможно использование моющих дезинфицирующих установок, разрешенных для применения в установленном порядке.
33. Стерилизация ИМН проводится путем обработки в горяче-воздушных стерилизаторах, автоклавах, погружения в растворы стерилизующих средств со спороцидным действием (дезинфекция высокого уровня) согласно методам, установленным в приложении 6 к настоящим Санитарным правилам.
34. Контроль качества стерилизации ИМН проводится согласно методам, установленным в приложении 7 к настоящим Санитарным правилам.
35. При проведении дезинфекции, предстерилизационной очистки и стерилизации растворами химических средств ИМН погружают в рабочий раствор дезсредства (далее – «раствор») с заполнением каналов и полостей. Разъемные изделия погружают в разобранном виде, инструменты с замковыми частями замачивают раскрытыми, сделав этими инструментами в растворе несколько рабочих движений.
36. Объём раствора для проведения обработки должен быть достаточным для обеспечения полного погружения ИМН, при этом объём раствора над изделиями должен быть не менее одного сантиметра (далее – см).
37. Дезинфекцию способом протирания допускается применять для тех ИМН, которые не соприкасаются непосредственно с пациентом или конструкционные особенности которых не позволяют применять способ погружения.
38. После дезинфекции ИМН многократного применения отмываются от остатков дезинфицирующего средства в соответствии с инструкцией (методическими рекомендациями) по его применению.
39. Контроль качества предстерилизационной очистки проводят ежедневно. Контролю подлежат: в стерилизационном отделении – 1 % от каждого наименования изделий, обработанных за смену; при децентрализованной обработке – 1 % одновременно обработанных изделий каждого наименования, но не менее трех единиц. Результаты контроля регистрируют в журнале.
40. Стерилизации подвергают все ИМН, контактирующие с раневой поверхностью, кровью (в организме пациента или вводимой в него) и/или инъекционными препаратами, а также отдельные виды медицинских инструментов, которые в процессе эксплуатации соприкасаются со слизистой оболочкой и могут вызвать ее повреждение.
41. Паровым методом стерилизуют ИМН, детали приборов, аппаратов из коррозионностойких металлов, стекла, бельё, перевязочный материал, изделия из резины, латекса и отдельных видов пластмасс.
42. Воздушным методом стерилизуют ИМН, детали приборов и аппаратов, в том числе изготовленные из коррозионно-нестойких металлов, изделия из силиконовой резины. Перед стерилизацией воздушным методом изделия после предстерилизационной очистки обязательно высушивают в сушильном шкафу при температуре 85 градусов Цельсия (далее - °С) до исчезновения видимой влаги. Использование сушильных шкафов (типа ШСС) для стерилизации воздушным методом запрещается.
43. Химический метод стерилизации с применением растворов химических средств применяют для стерилизации изделий, в конструкции которых использованы термолабильные материалы, не позволяющие использовать другие методы стерилизации.
Во избежание разбавления рабочих растворов погружаемые в них ИМН должны быть сухими.
При стерилизации растворами химических средств все манипуляции проводят строго соблюдая правила асептики: используют стерильные емкости для стерилизации и стерильную воду для отмывания изделий от остатков химических средств.
44. Газовым методом стерилизуют изделия из различных, в том числе термолабильных материалов, используя в качестве стерилизующих средств окись этилена, формальдегид, озон. Перед стерилизацией газовым методом с изделий после предстерилизационной очистки удаляют видимую влагу. Стерилизацию осуществляют в соответствии с режимами применения средств для стерилизации конкретных групп изделий, а также согласно инструкциям по эксплуатации стерилизаторов.
45. Плазменным методом, используя стерилизующие средства на основе перекиси водорода в плазменных стерилизаторах, стерилизуют хирургические, эндоскопические инструменты, эндоскопы, оптические устройства и приспособления, волоконные световодные кабели, зонды и датчики, электропроводные шнуры и кабели, другие изделия из металлов, латекса, пластмасс, стекла и кремния.
46. В стоматологических организациях (кабинетах) допускается применять гласперленовые стерилизаторы, в которых стерилизуют боры различного вида и другие мелкие инструменты при полном погружении их в среду нагретых стеклянных шариков. Не рекомендуется использовать данный метод для стерилизации рабочих частей более крупных стоматологических инструментов, которые невозможно полностью погрузить в среду нагретых стеклянных шариков.
47. Инфракрасным методом стерилизуют стоматологические инструменты из металла.
48. При паровом, воздушном, газовом и плазменном методах изделия стерилизуют в упакованном виде, используя бумажные, комбинированные и пластиковые стерилизационные упаковочные материалы, а также пергамент и бязь (в зависимости от метода стерилизации). Упаковочные материалы используются однократно.
При паровом методе, кроме того, используют стерилизационные коробки с фильтрами.
При воздушном и инфракрасном методах допускается стерилизация инструментов в неупакованном виде (в открытых лотках), после чего их сразу используют по назначению.
49. Хранение изделий, простерилизованных в упакованном виде, осуществляют в шкафах, рабочих столах. Сроки хранения указываются на упаковке и определяются видом упаковочного материала согласно инструкции по его применению.
50. Стерилизация изделий в неупакованном виде допускается только при децентрализованной системе обработки в следующих случаях:
1) при стерилизации ИМН растворами химических средств;
2) при стерилизации металлических инструментов термическими методами (гласперленовый, инфракрасный, воздушный, паровой) в портативных стерилизаторах.
Все изделия, простерилизованные в неупакованном виде, целесообразно сразу использовать по назначению. Запрещается перенос их из кабинета в кабинет.
51. При необходимости инструменты, простерилизованные в неупакованном виде одним из термических методов, после стерилизации допускается хранить в бактерицидных (оснащенных ультрафиолетовыми лампами) камерах в течение срока, указанного в руководстве по эксплуатации оборудования, а в случае отсутствия таких камер - на стерильном столе не более 6 часов.
52. ИМН, простерилизованные в стерилизационных коробках, допускается использовать не более чем в течение 6 часов после их вскрытия.
53. Бактерицидные камеры, оснащенные ультрафиолетовыми лампами, применяются только с целью хранения инструментов для снижения риска их вторичной контаминации микроорганизмами в соответствии с инструкцией по эксплуатации. Категорически запрещается применять такое оборудование с целью дезинфекции или стерилизации изделий.
54. При стерилизации изделий в неупакованном виде воздушным методом не допускаются хранение простерилизованных изделий в воздушном стерилизаторе и их использование на следующий день после стерилизации.
55. При стерилизации химическим методом с применением растворов химических средств отмытые стерильной водой простерилизованные изделия используют сразу по назначению или помещают на хранение в стерильную стерилизационную коробку с фильтром, выложенную стерильной простыней, на срок не более 3 суток.
56. Все манипуляции по накрытию стерильного стола проводят в стерильном халате, маске и перчатках с использованием стерильных простыней. Обязательно делают отметку о дате и времени накрытия стерильного стола. Стерильный стол накрывают на 6 часов. Не использованные в течение этого срока материалы и инструменты со стерильного стола направляют на повторную стерилизацию.
57. Не допускается использование простерилизованных ИМН с истекшим сроком хранения после стерилизации.
58. Контроль стерилизации включает контроль работы стерилизаторов, проверку значений параметров режимов стерилизации и оценку ее эффективности.
Контроль работы стерилизаторов проводят физическим (с использованием контрольно-измерительных приборов), химическим (с использованием химических индикаторов) и бактериологическим (с использованием биологических индикаторов) методами. Параметры режимов стерилизации контролируют физическим и химическим методами.
Эффективность стерилизации оценивают на основании результатов бактериологических исследований при контроле стерильности ИМН.
59. Стерилизаторы подлежат бактериологическому контролю после их установки (ремонта), а также в ходе эксплуатации не реже двух раз в год в порядке производственного контроля.
60. Техническое обслуживание, гарантийный и текущий ремонт стерилизаторов осуществляют специалисты сервисных служб.
61. Контроль работы паровых и воздушных стерилизаторов осуществляется физическими, химическими и бактериологическими методами с использованием химических и биологических тестов, термохимических индикаторов.
62. Физическим и химическим методами осуществляется контроль параметров режима работы паровых и воздушных стерилизаторов в процессе стерилизационного цикла, бактериологическим методом оценивается эффективность работы стерилизатора.
63. Контроль работы стерилизаторов проводится специалистами организации здравоохранения при каждой его загрузке.
64. Средства измерений стерилизационного оборудования подвергаются поверке в порядке, установленном законодательством Республики Казахстан.
65. Территориальными органами государственного санитарно-эпидемиологического надзора осуществляется выборочный контроль эффективности работы стерилизаторов.
66. При проведении контроля температуры стерилизатора, тесты (химические тесты, термохимические индикаторы и биологические тесты) упаковывают в пакеты из упаковочной бумаги со стерилизуемым материалом и размещают в контрольных точках стерилизатора согласноприложению 8 к настоящим Санитарным правилам.
67. Каждая партия стерилизуемого материала регистрируется в журнале учета стерилизации изделий медицинского назначения установленной формы согласно приложению 9 к настоящим Санитарным правилам. Паспорт стерилизатора, акты, протоколы проверки технического состояния стерилизаторов и эффективности стерилизации хранятся у ответственного лица в организации здравоохранения.
68. Эндоскопы, используемые при нестерильных эндоскопических манипуляциях (введение эндоскопов через естественные пути в полости организма, имеющие собственный микробный пейзаж), непосредственно после использования подлежат предварительной очистке, окончательной очистке, дезинфекции высокого уровня и хранению в условиях, исключающих вторичную контаминацию микроорганизмами.
Эндоскопы, используемые при стерильных эндоскопических манипуляциях (введение через их каналы стерильных инструментов, используемых при хирургических вмешательствах, введение эндоскопов в стерильные полости, контакт с раневой поверхностью, кровью), непосредственно после использования подлежат предварительной очистке, предстерилизационной очистке, стерилизации и хранению в условиях, исключающих вторичную контаминацию микроорганизмами.
Дезинфекция и стерилизация эндоскопов и инструментов к ним проводятся согласно приложению 10 к настоящим Санитарным правилам.
69. Ответственность за организацию и качество стерилизации ИМН возлагается на руководителя организации здравоохранения.
70. Физический метод контроля работы стерилизаторов осуществляют с помощью средств измерения температуры (термометр, термометр максимальный), давления (манометр) и учета времени стерилизации. Параметры режима работы стерилизатора следует проверять в течение всего цикла стерилизации, проводимой в соответствии с паспортом аппарата.
71. Химический метод контроля осуществляют с помощью химических тестов и термохимических индикаторов. Окончание стерилизации визуально определяется по изменению цвета индикаторов.
72. Бактериологический метод контроля осуществляют с помощью биологических тестов, содержащих дозированное количество спор микробов. Биологические тесты готовятся бактериологическими лабораториями центров санитарно-эпидемиологической экспертизы.
73. По окончании стерилизации биологические тесты помещают в полиэтиленовый пакет и в тот же день доставляют в бактериологическую лабораторию с сопроводительным бланком.
74. К работе с паровыми стерилизаторами допускаются лица старше восемнадцати лет, имеющие удостоверение о сдаче технического минимума по обслуживанию паровых стерилизаторов.
75. Паровой стерилизатор устанавливается на расстоянии 0,8 метра (далее – м) от стен, шкафные стерилизаторы - на расстоянии 1,5 м. Пол в помещении покрывается материалом, не проводящим ток.
76. Каждый электрический стерилизатор присоединяется к электросети через рубильник или автоматический выключатель. Включение парового стерилизатора в штепсельную розетку запрещается. Рубильник или автоматический выключатель устанавливаются на расстоянии 1,6 м от пола и не далее 1 м от парового стерилизатора. Запрещается подключение к этому рубильнику или автоматическому выключателю других потребителей электроэнергии.
77. Запрещается использовать в качестве заземления водопроводные трубы сети центрального отопления, канализации, трубопроводы горючих или взрывчатых веществ, заземлители молниеотводов.
78. В помещении для паровых стерилизаторов должны соблюдаться правила пожарной безопасности. Запрещаются проведение в стерилизаторах каких-либо работ, не связанных со стерилизацией медицинских изделий, а также хранение в помещении посторонних предметов, загромождающих и загрязняющих помещение.
79. Вход в помещение во время работы стерилизаторов разрешается только обслуживающему персоналу и лицам, осуществляющим контроль за эксплуатацией стерилизаторов.
80. В каждом помещении, где установлена стерилизационная аппаратура, на видном месте располагаются правила по ее эксплуатации.
81. Паспорт завода-изготовителя на паровой стерилизатор хранится у лица, ответственного за состояние и безопасность парового стерилизатора.
82. Помещение автоклавной обеспечивается естественным освещением, приточно-вытяжной вентиляцией, фрамугами или форточками. Дверь в помещение во время работы стерилизатора не запирается.
83. Каждый паровой стерилизатор оснащается предохранительным клапаном и исправным запломбированным манометром, имеющим класс точности не менее двух с половиной и такую шкалу, чтобы предел измерения рабочего давления находился во второй трети шкалы.
84. Не допускается к применению манометр при отсутствии пломбы на клейме, просроченном сроке поверки, разбитом стекле или других повреждениях, в случае, когда стрелка манометра при его выключении не возвращается на нулевую отметку.
85. Предохранительный клапан должен быть отрегулирован на разряженное давление в стерилизаторе.
86. Обслуживающий персонал выполняет требования по режиму работы и безопасному обслуживанию паровых стерилизаторов, своевременно проверяет исправность контрольно-измерительных приборов и предохранительных устройств.
87. Ремонт паровых стерилизаторов проводится специалистами, имеющими соответствующее разрешение.
4. Организация и проведение дезинсекции
88. При поселковой дезинсекции работа на объектах начинается с их предварительного обследования на наличие насекомых, определения видов, выявления мест заселенности и численности. Выборочный контроль в дальнейшем осуществляют государственные органы санитарно-эпидемиологической службы.
89. Кратность обработок определяется особенностями биологии и экологией целевых видов, санитарным состоянием объектов и уровнем их заселенности насекомыми, характеристиками применяемых дезсредств.
90. Обработку необходимо проводить либо непосредственно перед выплодом (вылетом) насекомых, либо сразу после него.
91. Основным показателем эффективности поселковой дезинсекции считается прирост освобожденной от насекомых площади, а при борьбе с мухами – отсутствие личинок, куколок и снижение численности.
92. Применяются три типа обработки против насекомых и других членистоногих:
1) сплошная обработка – проводится при поселковой дезинсекции во всех заселенных целевыми видами насекомых помещениях и на прилегающих территориях;
2) барьерная обработка – создание защитных зон вокруг определенной территории. Проводится когда необходимо создать барьер, препятствующий проникновению насекомых на определенную территорию. При этом могут обрабатываться растительность в открытых стациях, норы грызунов, открытые водоемы и т. д. Ширина барьерной зоны определяется особенностями экологии целевых видов и угрожающей нозологии, а также дальностью массовых перемещений населения.
3) микроочаговая обработка – дезинсекция в очаге инфекционных заболеваний и на прилегающей к нему территории. Проводится при регистрации инфекционного заболевания, в распространении которого могут принимать участие насекомые.
93. При контрольном обследовании объект относят к «освобожденным от насекомых», если насекомые не наблюдаются в течение месяца ни в одном из помещений. При обнаружении даже единичных живых насекомых объект переводится в категорию «заселенных» и проводится повторная обработка.
94. Заселенность насекомыми зданий (или встроенных объектов) считается высокой, если отдельные насекомые и их скопления обнаружены более чем, на 20 % площади объекта. В этом случае обязательна сплошная обработка помещений.
95. В случае выявления неэффективности обработок, они проводятся повторно за счет исполнителя.
96. Обработка против комаров проводится непосредственно перед их вылетом с зимовок или перед вылетом первой генерации, в отапливаемых подвальных помещениях обработка проводится круглогодично.
97. Основным мероприятием в борьбе с мухами является обработка мест их выплода. Для уничтожения личинок и куколок мух почва обрабатывается ларвицидами на расстоянии 30-50 см и более до 80 см от краев мусоросборников, не канализованных уборных, асфальтированных площадок, окружающих санитарно-дворовые установки, скоплений навоза.
98. Регулярные деларвационные (направленные против личинок и куколок мух) работы начинаются весной при появлении личинок I и II стадий первой летней генерации и продолжаются в течение всего летнего периода. Для уничтожения личинок и куколок мух в мусоре, навозе, почве инсектициды используются, как правило, в виде растворов, эмульсий для лучшего проникновения их в обрабатываемый субстрат.
99. При проведении обработок открытых территорий против экзофильных видов, компонентов гнуса проводится деларвация всех прибрежных водоемов, мест массового выплода как на территории защищаемого объекта (населенный пункт, место работы большого коллектива людей), так и вокруг него (защитная зона). Ширина защитной зоны в зависимости от ландшафта, зарастаемости территории растительностью, дальности разлета гнуса имеет радиус от 1 до 6 км и более.
100. Критерием оценки эффективности выполненных противомушиных мероприятий является сезонный показатель численности комнатных и экзофильных видов мух. В городах удовлетворительным сезонным показателем численности комнатных мух является один экземпляр на 1 липкий стандартный лист (в сутки), экзофильных мух – 3-5 экземпляров на одну мухоловку; для сельской местности – 5 и 20 соответственно.
101. Учет численности проводится один раз в 3-10 дней в течение суток в период активности мух, в помещениях он должен проводится с помощью липких лент из расчета 1 на 20 квадратных метра (далее – м 2 ), в местах выплода – выловом в сетчатые мухоловки. Эффективность считается удовлетворительной при отсутствии окрыленных мух, при численности в среднем не более 1 экземпляра на 1 стандартный липкий лист (за сутки). Для участков с преобладающей индивидуальной застройкой при отсутствии канализации и для сельской местности – 3-5 экземпляров.
102. Контроль эффективности дезинсекционных мероприятий на объектах осуществляется специалистами государственной санитарно- эпидемиологической службы.
103. Определение эффективности мероприятий проводят путем учета численности окрыленных мух, а также личинок и куколок в местах выплода. Учету подлежит не менее 5 % обслуживаемых объектов в населенном пункте.
104. Истребительные мероприятия прекращаются, если насекомых не обнаруживают при контролях всеми методами в течение месяца после обработок.
105. Контроль эффективности дезинсекционных мероприятий на объектах от комаров осуществляется в сроки, определяемые используемым дезсредством, типом обрабатываемых поверхностей. Эффективность считается удовлетворительной при регистрации единичных экземпляров, учет ведется в течение 20 минут «методом открытых рук».
106. Основным показателем эффективности противоличиночных мероприятий является численность окрыленных комаров в защищенных объектах, обнаружение на 5-7 сутки после обработок личинок и комаров имаго должно быть не более 1 особи окрыленных комаров на 1 м 2 подвала.
107. Критерием оценки эффективности противогнусовых и противоклещевых мероприятий на открытых территориях, обработки нор грызунов при создании защитных зон является гибель не менее 80 % насекомых (клещей) через сутки после обработки при 100 % охвате территории, подлежащей дезинсекции (деакаризации).
108. Показателем эффективности дезинсекции в отношении подвальных комаров являются отсутствие на 3-5 сутки после обработок живых личинок в пробах и наличие в среднем не более 1 особи окрыленных комаров на 1 м 2 .
109. При оценке эффективности мероприятий по уничтожению блох в помещениях используются липкие листы (20×30 см) из расчета 2 листа на 10 м 2 поверхности пола. Если на 1 лист в течение суток попало не более 2 блох, считают, что насекомые «единичные», от 3 до 10 – «блох много», более 10 – «очень много».
110. При оценке эффективности мероприятий по уничтожению постельных клопов осматриваются наиболее вероятные места их нахождения, результаты осмотра записываются следующим образом: «единичные насекомые», «скопления насекомых», а при отсутствии клопов – «насекомые не обнаружены».
111. При оценке эффективности противопедикулезных мероприятий удовлетворительным ее показателем считается полное отсутствие насекомых и гнид после обработки.
5. Организация и проведение дератизации
112. Дератизация осуществляется с целью уничтожения грызунов и освобождения от них заселенных объектов или для постоянного поддержания их численности на минимальном уровне, обеспечивающем предотвращение широкого распространения инфекционных болезней и существенного экономического ущерба.
113. Поселковая дератизация подразделяется на следующие типы:
1) сплошная дератизация – проводится на территории всего населенного пункта, включая открытые места обитания в его пределах, не реже 2 раз в год;
2) очаговая дератизация – дератизация в очаге инфекционных заболеваний и на прилегающей к нему территории. Проводится при регистрации инфекционного заболевания, в распространении которого могут принимать участие грызуны.
3) выборочная дератизация – проводится, когда необходимо провести уничтожение грызунов на отдельных участках или строениях, в основном на эпидемически значимых объектах: мясо- и рыбокомбинатах, холодильниках, элеваторах, продовольственных складах, в лечебных и детских учреждениях, на животноводческих фермах.
114. Дератизацию проводят физическими, механическими, химическими способами, методами раскладки отравленных приманок, опыливания, газации. Выбор способа и метода дератизации определяется особенностями обрабатываемого объекта, экологией целевых грызунов и свойствами дератизационных средств.
115. Обследованию на наличие грызунов подлежит вся площадь строений и территорий организаций здравоохранения, детских организаций, объектов общественного питания, продовольственной торговли один раз в квартал.
116. Для обеспечения эффективности профилактических дератизационных работ предусматривается соблюдение определенной кратности обработок. Если инструкцией по применению используемого препарата не рекомендуется иное, то дератизацию помещений проводят 1 раз в 2-3 месяца, дератизацию территории – 4-6 раз в год. При длительном отсутствии грызунов помещения исключают из обработки, а количество обработок территории сокращают вдвое.
117. Отравленная приманка на объектах продовольственной торговли, общественного питания, овощехранилищах, складах, жилых помещениях и надворных постройках раскладывается в соответствии с режимом применения, предусмотренным в инструкциях по использованию дератизационных средств. В помещениях детских организаций, в которые имеют доступ дети, раскладка отравленной приманки не допускается, а уничтожение грызунов производится исключительно механическими методами.
118. Средства дератизации должны внешне резко отличаться от пищевых продуктов, фуража, предметов домашнего обихода, лекарственных препаратов. В качестве пищевой основы приманок запрещается использовать недробленые семена подсолнуха и иные продукты, имеющие привлекательный для людей вид. Во избежание несчастных случаев родентицидную приманку для грызунов необходимо окрашивать в яркий цвет.
119. Отравленная приманка на открытых территориях раскладывается только скрытно и должна быть недоступна детям, домашним животным и птицам.
120. Работы по приготовлению приманок должны быть максимально механизированы с применением специальных смесителей. Приготовление и фасовка отравленных приманок должны проводиться под вытяжкой и с соблюдением мер безопасности, указанных в соответствующих инструкциях на конкретные дератизационные средства.121. В рабочих помещениях по приготовлению приманок проводится периодический контроль воздуха на содержание действующего вещества родентицида.122. В помещениях, где имеются незатаренные пищевые продукты, запрещается применять сыпучие (в том числе зерновые) отравленные приманки и использовать средства дератизации в форме дустов.123. В помещениях, где постоянно бывают люди, после завершения дератизации все остатки приманки с ядом должны быть собраны с целью утилизации. В местах, недоступных детям и домашним животным, приманка оставляется для предотвращения вселения грызунов на защищаемый объект.
124. Эффективность дератизации достигается:
1) проведением на объекте санитарного дня для проведения сплошной обработки всех заселенных грызунами помещений;
2) соблюдением технологии раскладки приманки, предусмотренной инструкцией по ее применению;
3) обеспечением в складских помещениях постоянного доступа к стенам, углам и техническим вводам для лиц, проводящих дератизацию, путем устройства прохода вдоль стен шириной не менее 70 см;
4) оборудованием стеллажей, отстоящих от пола не менее чем на 15 см во всех местах хранения различных материалов;
5) хранением продуктов и запасов воды в условиях, максимально затруднявших доступ грызунов к ним:
6) обеспечением доступа для лиц, проводящих дератизацию, во все помещения до их загрузки для проведения профилактической обработки;
7) соблюдением правил грызунонепроницаемости зданий и помещений;
8) проведением регулярной уборки во всех помещениях и на прилегающей к ним территории и вывозом мусора в установленные сроки.
125. При проведении сплошной дератизации в населенном пункте его население обязательно оповещается об этом через средства массовой информации.
126. Населенный пункт или его часть делят на участки, которые нумеруют и наносят на схематическую карту. Размеры участка определяют, исходя из объема работ. Каждый участок закрепляют за конкретным дератизатором.
127. Заселенные грызунами строения дератизатор посещает два раза в месяц или чаще, исходя из конкретных условий. По мере повышения эффективности дератизации кратность посещения дератизатором свободных от грызунов строений уменьшают.
128. При появлении инфекционного заболевания, связанного с грызунами, помимо осуществления перечисленных выше мер проводят дератизационные мероприятия по типу экстренной профилактики: применяют остродействующие ратициды в составе отравленных пищевых приманок, содержащих растительное масло в качестве атграктанта.
129. Основным принципом наиболее эффективной методики борьбы с синантропными грызунами являются применение средств борьбы во всех без исключения местах обитания грызунов и непрерывность этого воздействия.
130. В качестве основного средства борьбы необходимо применять долго сохраняющиеся приманки с антикоагулянтами, а приманки с остродействующими ядами не чаще двух раз в год в период осеннего пика численности и весеннего размножения грызунов, а также по эпидпоказаниям.
131. Давилки, капканы и другие ловушки рекомендуется применять на отдельных объектах в качестве дополнительного метода дератизации.
132. Применять яды для опыливания нор и троп грызунов следует в небольшом объеме, так как этот способ приводит к сильному загрязнению пестицидами окружающей среды и повышает опасность проводимых работ для лиц, постоянно находящихся в обработанном помещении.
133. Бактериальные препараты против грызунов в населенных пунктах применяются только по разрешению территориального органа государственного санитарно-эпидемиологического надзора.
134. Особое внимание уделяется применению сухих приманок с антикоагулянтами при систематической обработке строений, легко доступных для грызунов и повторно заселяемых ими. На таких объектах сухие приманки находятся постоянно.
135. Важным условием проведения качественной дератизации является использование в отравленных приманках разных привлекательных для грызунов продуктов: муки, зерна, крупы, сахара, растительного масла, реже хлеба, овощей, мясных и рыбных отходов.
136. Контроль за ходом дератизационных мероприятий осуществляется специалистами органов государственного санитарно-эпидемиологического надзора.
137. Показателем качества дератизации является учет численности грызунов с применением орудий лова, который проводится через 15-45 дней (в зависимости от использованных средств) после проведения дератизации. Охвату подлежит 1-5 % обработанных объектов.
138. Дератизация в населенном пункте признается эффективной при гибели не менее 80 % грызунов.
к Санитарным правилам