










 Рейтинг: 4.9/5.0 (1847 проголосовавших)
Рейтинг: 4.9/5.0 (1847 проголосовавших)Категория: Инструкции
4 упаковки -3850 евро каждая
5 упаковок -3800 евро каждая
10 упаковок -3700 евро каждая
20 упаковок -3650 евро каждая
30 упаковок -3600 евро каждая
40 упаковок -3500 евро каждая
Адцетрис купить в МосквеAdcetris (Адцетрис) по доступной цене можно заказать у нашего представителя в Москве 89258767555 Антон. Лекарство Адцетрис покупаем в Германии
Сотовый номер +4915739803419 или +7(963) 65-86-777 Александр Мюллер
Адцетрис доставляем из Германии в холодильнике в Москву и по все России бесплатно
Действующее вещество:
Брентуксимаб (Brentuximab vedotin)
Форма выпуска:
Порошок для приготовления концентрата для раствора для инфузий 50 мг
Фармакотерапевтическая группа
Противоопухолевые препараты. Противоопухолевые препараты. Моноклональные антитела. Брентуксимаб ведотин
Показания:
для лечения взрослых пациентов с рецидивирующей или рефрактерной формой CD30-положительной лимфомой Ходжкина (ЛХ):
После трансплантации аутологичных стволовых клеток (ТАСК)
После, как минимум, двух курсов терапии с помощью ТАСКили химиотерапии с использованием нескольких лекарственных средств.
Для лечения взрослых пациентов с рецидивирующей или рефрактерной системной анапластической крупно клеточной лимфомой (сАККЛ)
Способ применения и дозы
Адцетрис необходимо применять под наблюдением врача, имеющего опыт применения противоопухолевых лекарственных средств.
Дозы
Рекомендуемая доза составляет 1,8 мг/кг в виде 30-минутноговнутривенного введения каждые 3 недели.
Противопоказания
Повышенная чувствительность к активному веществу или другим компонентам препарата
Одновременное применение блеомицина и Адцетрис (вызывает легочную токсичность)
Рекомендуемая доза составляет 1.8 мг/кг в виде 30-минутного в/в введения каждые 3 недели.
Если масса тела пациента составляет более 100 кг, то для расчета дозы следует использовать 100 кг. Во время курса лечения необходимо проводить полный анализ крови перед применением каждой дозы. Во время и после введения препарата за пациентами необходимо вести наблюдение. Лечение необходимо продолжать до тех пор, пока не будут наблюдаться прогрессирование заболевания или недопустимая токсичность. Пациенты, достигающие стабильной фазы заболевания или улучшения состояния, должны получить, как минимум, 8 циклов и, как максимум, 16 циклов лечения (примерно в течение одного года).
Если в период лечения развивается нейтропения, то необходимо провести коррекцию режима дозирования в соответствии со специальными рекомендациями.
Инфекции: инфекции верхних дыхательных путей, опоясывающий герпес (лишай), пневмония; кандидоз ротовой полости, пневмония, вызванная Pneumocystis jiroveci, стафилококковая бактериемия.
Со стороны системы кроветворения: нейтропения; анемия, тромбоцитопения; фебрильная нейтропения.
Со стороны нервной системы: периферическая сенсорная невропатия; периферическая моторная невропатия, головокружение, демиелинизирующая полиневропатия, прогрессивная мультифокальная лейкоэнцефалопатия (ПМЛ).
Со стороны пищеварительной системы: диарея, тошнота, рвота, запор.
Со стороны кожи и подкожно-жировой клетчатки: алопеция, зуд, сыпь, синдром Стивенса-Джонсона.
Со стороны костно-мышечной системы: миалгия, артралгия, боль в пояснице.
Со стороны дыхательной системы: кашель, одышка.
Со стороны обмена веществ: гипергликемия.
Аллергические реакции: анафилактическая реакция.
Иммунологические реакции: антитела к бентуксимабу ведотину.
Общие реакции: утомляемость, пирексия, озноб, синдром лизиса опухоли.
Реакции, связанные с инфузией: озноб, тошнота, одышка, зуд, кашель.
Противопоказания к применению
Одновременное применение блеомицина и брентуксимаба ведотина (вызывает легочную токсичность), повышенная чувствительность к активному веществу.
Применение при беременности и кормлении грудью
Клинических данных о применении брентуксимаба ведотина при беременности нет. Исследования на животных показали репродуктивную токсичность. Брентуксимаб ведотин не следует применять при беременности за исключением случаев, когда ожидаемая польза терапии для матери превышает потенциальный риск для плода. В случае необходимости применения при беременности пациентку следует проинформировать о потенциальном риске для плода.
Неизвестно, выделяются ли брентуксимаб ведотин и его метаболиты с грудным молоком. Нельзя исключить риск для детей, находящихся на грудном вскармливании. При необходимости применения в период лактации грудное вскармливание следует прекратить.
Женщинам детородного возраста необходимо использовать надежный способ контрацепции в период лечения и в течение до 30 дней после лечения.
Лечение брентуксимабом ведотином может вызвать реактивацию JC вируса (вирус Джона Канингема), который вызывает развитие ПМЛ и приводит к смерти. Возникновение ПМЛ отмечали у пациентов, получавших брентуксимаб ведотин после нескольких курсов химиотерапии. ПМЛ — это редкое демиелинизирующее заболевание ЦНС, которое возникает в результате реактивации латентного JC вируса и часто заканчивается смертью.
Необходим строгий клинический контроль с целью выявления любых новых или обострения существующих неврологических, когнитивных или поведенческих симптомов, которые могут указывать на развитие ПМЛ. Лечение брентуксимабом ведотином следует приостановить при подозрении на ПМЛ и провести соответствующее обследование.
На фоне лечения брентуксимабом ведотином были зарегистрированы случаи острого панкреатита с летальным исходом. При появлении или прогрессировании боли в животе следует провести обследование для исключения острого панкреатита.
У пациентов, получающих брентуксимаба ведотин, были зарегистрированы случаи легочной токсичности. Хотя причинно-следственная связь с брентуксимабом ведотином не была установлена, не следует исключать риск возможного возникновения легочной токсичности. В случае появления новых или ухудшения имеющихся легочных симптомов (например, кашель, одышка) следует провести соответствующее обследование и назначить лечение.
В случае возникновения серьезных и оппортунистических инфекций необходим клинический контроль.
Во время проведения и после завершения инфузии пациенты должны находиться под наблюдением врача. При анафилаксии введение брентуксимаба ведотина следует немедленно прекратить и назначить соответствующее лечение.
Реакции на инфузию проявляются чаще и сильнее у пациентов с антителами к брентуксимабу ведотину.
Пациенты с быстро пролиферирующей опухолью относятся к группе риска по развитию синдрома лизиса опухоли. В таких случаях требуется клинический контроль и проведение соответствующей терапии.
Пациенты должны находиться под наблюдением врача с целью своевременного выявления таких симптомов невропатии, как гипестезия, гиперестезия, парестезия, дискомфорт, жжение, нейропатическая боль или слабость. В случае возникновения или обострения периферической невропатии необходимо приостановить лечение и снизить дозу или полностью прекратить лечение.
Перед каждой инфузией необходимо проводить развернутый анализ крови.
При развитии на фоне лечения синдрома Стивенса-Джонсона или токсического эпидермального некролиза брентуксимаб ведотин следует отменить.
Известны случаи развития гипергликемии при проведении клинических исследований у пациентов с повышенным ИМТ, с или без сахарного диабета в анамнезе. Однако необходимо внимательно следить за уровнем глюкозы в плазме крови, если у пациента выявлена гипергликемия. Следует назначить соответствующие гипогликемические препараты.
По данным доклинических исследований, лечение брентуксимабом ведотином вызывает токсическое поражение яичек и может привести к нарушению фертильности у мужчин. Исследования также показали, что брентуксимаб ведотин обладает анетигенными свойствами. Перед началом лечения брентуксимабом ведотином мужчинам рекомендуется заморозить образцы спермы для хранения. Мужчинам не рекомендуется планировать зачатие во время лечения и в течение 6 месяцев после введения последней дозы.
Влияние на способность к вождению автотранспорта и управлению механизмами
Брентуксимаб ведотин может в незначительной степени влиять на скорость реакции при управлении транспортным средством или работе с другими потенциально опасными механизмами.
Одновременное применение брентуксимаба ведотина с кетоконазолом, мощным ингибитором CYP3A4 и Р-гликопротеина, привело к усилению интенсивности действия брентуксимаба ведотина приблизительно на 73% и не повлияло на его концентрацию в плазме крови. Поэтому при одновременном применении брентуксимаба ведотина с мощными ингибиторами CYP3A4 и P-гликопротеином возрастает риск возникновения нейтропении.
Применение брентуксимаба ведотина в комбинации с рифампицином, мощным ингибитором CYP3A4, не повлияло на концентрацию брентуксимаба ведотина в плазме крови, но привело к уменьшению интенсивности действия брентуксимаба ведотина примерно на 31%.



Информация о препаратах, отпускаемых по рецепту, размещенная на сайте, предназначена только для специалистов. Информация, содержащаяся на сайте, не должна использоваться пациентами для принятия самостоятельного решения о применении представленных лекарственных препаратов и не может служить заменой очной консультации врача.
Copyright © Справочник Видаль «Лекарственные препараты в России»

![]()
Adcetris используется для лечения лимфомы Ходжкина или анапластической крупноклеточной лимфомы. Adcetris применяется после трансплантации стволовых клеток или, когда другие лекаhttp://likitoriya.com/goods/adcetris.html рства были опробованы без успешного лечения. Адцетрис применяется для лечения взрослых пациентов с рецидивной или рефрактерной системной анапластической крупноклеточной лимфомой.
Условия храненияпри температуре 2–8 °C в оригинаhttp://likitoriya.com/goods/adcetris.html льной упаковке. Не замораживать.
Москва, Санкт-Петербург, Екатеринбург, Казань, Саратов, Пермь, Воронеж, Красноярск, Уфа, Омск, Волгоград, Барнаул, Хабаровск, Иркутск, Калининград, Владивосток, Тула, Тюмень, Ижевск, Томск, Пенза, Оренбург, Ульяновск, Йошкар-Ола, Тольятти, Кемерово, Ярославль, Рязань, Ставрополь, Липетск, Мурманск, Курск, Сургут, Смоленск, Абакан, Новокузнецк, Орел, Калуга, Магнитогорск, Сочи, Киров, Кострома, Астрахань, Пятигорск. Перечень постоянно дополняется, спрашивайте консультанта, если Вашего города нет в списке
Смотрите также аналоги:Известных аналогов нет
Каталог лекарствАдцетрис можно купить в Москве у нашего представителя
Латинское название:
Adcetris
Действующее вещество:
Брентуксимаб (Brentuximab vedotin)
Форма выпуска:
Порошок для приготовления концентрата для раствора для инфузий 50 мг
Производитель:
TAKEDA (Германия)
Фармакотерапевтическая группа
Противоопухолевые препараты. Противоопухолевые препараты. Моноклональные антитела. Брентуксимаб ведотин
Показания:
для лечения взрослых пациентов с рецидивирующей или рефрактерной формой CD30-положительной лимфомой Ходжкина (ЛХ):
После трансплантации аутологичных стволовых клеток (ТАСК)
После, как минимум, двух курсов терапии с помощью ТАСКили химиотерапии с использованием нескольких лекарственных средств.
Для лечения взрослых пациентов с рецидивирующей или рефрактерной системной анапластической крупно клеточной лимфомой (сАККЛ)
Способ применения и дозы
Адцетрис необходимо применять под наблюдением врача, имеющего опыт применения противоопухолевых лекарственных средств.
Дозы
Рекомендуемая доза составляет 1,8 мг/кг в виде 30-минутноговнутривенного введения каждые 3 недели.
Противопоказания
Повышенная чувствительность к активному веществу или другим компонентам препарата
Одновременное применение блеомицина и Адцетрис (вызывает легочную токсичность)
Если масса тела пациента составляет более 100 кг, то для расчета дозы следует использовать 100 кг. Во время курса лечения необходимо проводить полный анализ крови перед применением каждой дозы. Во время и после введения препарата за пациентами необходимо вести наблюдение. Лечение необходимо продолжать до тех пор, пока не будут наблюдаться прогрессирование заболевания или недопустимая токсичность. Пациенты, достигающие стабильной фазы заболевания или улучшения состояния, должны получить, как минимум, 8 циклов и,как максимум, 16 циклов лечения (примерно в течение одного года).
Препарат Адцетрис предназначен для взрослых пациентов, страдающих рецидивной или резистентной CD30 позитивной лимфомой Ходжкина. Лекарственное средство показано больным, которым были трансплантированы аутологические стволовые клетки, а также получавшим лечение как минимум дважды другими препаратами. Также Адцетрис можно назначать пациентам, которым не помогла трансплантация аутологических стволовых клеток или химиотерапия несколькими веществами. Показанием к применению препарата является и рецидивная или резистентная систематическая анапластическая крупноклеточная лимфома у взрослых пациентов.
Страдающему от редкой и агрессивной формы рака жителю Великобритании Яну Бруксу, тело которого поразили около 70 злокачественных опухолей, по самым оптимистичным прогнозам врачей оставалось жить всего несколько недель.
Медики признали, что перепробовали практически все варианты лечения. Однако, несмотря на неутешительные прогнозы, 47-летний Брукс в настоящее время находится в состоянии полной ремиссии после того, как стал первым человеком, испробовавшим на себе новый противораковый препарат.
На снимках видно, как сильно по телу мужчины распространился рак. Однако второе сканирование, сделанное всего через нескольких недель после приема нового препарата, показало удивительное улучшение.
Снимки, сделанные "до" и "после" лечения
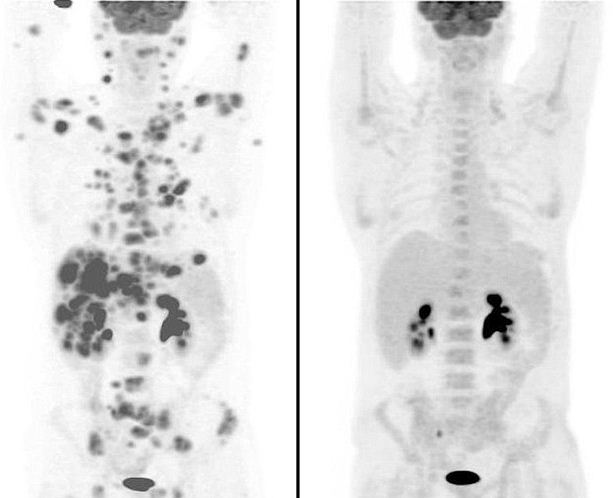
Все опухоли были уничтожены. Единственные темные пятна, видимые на снимках, демонстрируют нормальное функционирование почек и мочевого пузыря.
Клиническое испытание в больнице Кристи в Манчестере оказалось настолько успешным, что препарат было решено испробовать и на других больных. Теперь пациенты с той же редкой формой неходжкинской лимфомы – разновидностью рака, которая поражает лимфатические узлы, также будут получать лекарство.
"Я не думаю, что был бы здесь сегодня без этого препарата. Мой лечащий врач был так взволнован, когда увидел результаты, что незамедлительно показал их и мне. У меня было 70 опухолей и все они исчезли", - сказал в интервью Mail Online Брукс, автослесарь из Болтона.

У мужчины была редкая форма рака, которая называется анапластической крупноклеточной неходжкинской лимфомой. Заболевание у него было диагностировано в 2001-м году и сначала хорошо поддавалось лечению, но в 2008-м - вернулось. Мужчина перенес операцию по трансплантации стволовых клеток, но рак снова вернулся, начав быстро распространяться.
Учитывая то, что по мнению врачей ему оставалось жить всего несколько недель, Брукс решил принять участие в клинических испытаниях. Состояние больного начало улучшаться уже в течение первых 24 часов после начала приема препарата и врачи крупнейшего центра рака в Европе были поражены, увидев результаты сканирования.
Всего лишь после 12 недель лечения онкологи обнаружили, что его тело полностью избавилось от опухолей. По их мнению, в данный момент Брукс находится в состоянии полной ремиссии.
ОтзывыАдцетрис цена в Москве будет такая же как и в аптеках Германии. Но если вы прилетаете к нам в Германию, мы сделаем вам скидку на препарат Адцетрис. Адцетрис доставка из германии в Москву на самолете, поддерживая нужную температуру от 2 до 8 градусов, в термосумке с аккумулятором холода. если вы хотите купить адцетрис дешево, доставить срочно, то вам нужно обратиться к нам на электронный адрес pillsgermany@mail.ru
Торговое названиеМеждународное непатентованное название
Лекарственная формаПорошок для приготовления концентрата для раствора дляинфузий 50 мг
Один флакон содержит
активное вещество – брентуксимаба ведотина 50 мг,
вспомогательные вещества: кислота лимонная моногидрат,натрия цитрата дигидрат, a,a-трегалозы дигидрат, полисорбат 80.
Показания к применениюдля лечения взрослых пациентов с рецидивирующей илирефрактерной формой CD30-положительной лимфомой Ходжкина (ЛХ):
1) послетрансплантации аутологичных стволовых клеток (ТАСК); или
2) после, как минимум, двух курсов терапии с помощью ТАСКили химиотерапии с использованием нескольких лекарственных средств.
для лечения взрослых пациентов с рецидивирующей илирефрактерной системной анапластической крупноклеточной лимфомой
автор Артур Шмидт
Адцетрис 50мг (ADCETRIS 50MG) в упаковке 1 шт.,цена вместе с доставкой:
1 упаковка - 4000 евро
2 упаковки - 3950 евро каждая
3 упаковки - 3900 евро каждая
Теперь вы можете заказать препараты у наших представителей в Москве, оплата на месте. При покупке через наших представителей лекарства ценовой категории до 500 евро будет + 5 евро за упаковку, до 1000 евро будет + 10 евро за упаковку. Повышение цен обусловлено тем, что представители приобретают заказанные препараты за свой счет.
Наши представители в Москве:
Способы и сроки доставки следующие:
Данный препарат нужно перевозить строго в холодильнике поддерживая нужную температуру. Мы можем доставить eгo в течение 2-x дней в Москву, Минск и Киев в мини холодильнике со льдом. Такая доставка стоит 80 евро, 130 евро по всей России
Наши контакты в Германии:

Адцетрис - Инструкция по применению
Произношение
на русском языке: Адцетрис
на английском языке: Adcetris
Лекарственная форма. инъекции, порошок, lyophilized для решения
ПОЛНАЯ ПРЕДПИСЫВАЮЩЕЕ ИНФОРМАЦИЯ
Показания и использование для Adcetris
Эти показатели основываются на количество ответов. Нет данных демонстрации улучшения в пациент сообщили результаты или выживание с Adcetris.
Лимфома Ходжкина
Adcetris (brentuximab vedotin) указывается для лечения больных с лимфомой Ходжкина (HL) после трансплантации аутологических стволовых клеток, что (ASCT) или после сбоя по меньшей мере два ранее многоагентных химиотерапии схемы терапии у пациентов, которые не являются кандидатами на ASCT.
Системные анапластические большой клеточная лимфома
Adcetris указано для лечения больных с системной анапластические большой клеточная лимфома (sALCL) после сбоя по крайней мере один режим предварительного многоагентных химиотерапии.
Дозировка Adcetris и управление
Общая информация дозирования
Рекомендуемая доза составляет 1,8 мг/кг только как внутривенное вливание свыше 30 минут каждые 3 недели.
Не управлять как внутривенное толчок или струйное вливание.
Продолжать лечение до максимум 16 циклов, развитие болезни или неприемлемые токсичности.
Модификация доза
Периферийная невропатия: Периферийная невропатия должно осуществляться с помощью комбинации доза задержки и сокращение до 1,2 мг/кг. Для новых или ухудшение класса 2 или 3 невропатия дозирование должен быть до невропатия улучшает для 1 класса или базовой линии и затем перезапустить на 1,2 мг/кг. Для 4 класса периферической невропатии необходимо прекратить Adcetris.
Нейтропения. Нейтропения должны управляться доза задержек и сокращений. Доза Adcetris следует проводить для класса 3 или 4 нейтропения до разрешения для базового или класса 2 или меньше. Фактор роста поддержки следует рассматривать для последующих циклов в пациентах, которые испытывают класса 3 или 4 нейтропения. У больных с периодических нейтропения уровня 4, несмотря на использование факторов роста можно считать прекращения или уменьшения дозы Adcetris to1.2 мг/кг.
Инструкции для подготовки и управления
Следует рассмотреть процедуры для надлежащей обработки и утилизации противораковых лекарств.
Соответствующие асептических метод используйте для воссоздания и подготовка дозирования решений.
Рассчитать доза (мг) и количество флаконов Adcetris требуется. Доза для пациентов с весом > 100 кг должны быть рассчитаны на 100 кг. Восстановить каждый 50 мг флакона Adcetris с 10,5 мл стерильного воды для инъекций, USP, для получения одноразового раствор, содержащий 5 мг/мл brentuximab vedotin. Прямой поток к стене флакона и непосредственно не на торт или порошка. Аккуратно вихревой флакона для роспуска. НЕ ПОКОЛЕБАТЬ. Проверьте водостойких решение для твердых частиц и обесцвечивание. Воссозданная решение должно быть ясно слегка опалесцирующая, бесцветные и свободной от видимых частиц. После воссоздания сразу же ослабить в инфузии мешок, или хранить решение в 2-8?C (36-46?F) и использовать в течение 24 часов с момента воссоздания. НЕ ЗАМОРАЖИВАТЬ. Отменить любые неиспользованную часть оставил во Флаконе.
Расчете необходимый объем 5 мг/мл воссоздана необходимые решения Adcetris и вывести эту сумму из флаконов. Доза для пациентов с весом > 100 кг должны быть рассчитаны на 100 кг. Сразу же добавьте водостойких решение в инфузии пакет, содержащий минимальный объем 100 мл для достижения окончательного концентрацию 0,4 мг/мл до 1,8 мг/мл brentuximab vedotin. Adcetris могут быть ослаблены в 0.9% натрия хлорида раствор для инъекций, 5% декстроза инъекций или Lactated Ringer инъекции. Аккуратно инвертировать мешка перемешать решения. Adcetris содержит консерванты бактериостатическим. После разрежения влить Adcetris решение немедленно, или хранить решение в 2-8?C (36-46?F) и использовать в течение 24 часов с момента воссоздания. НЕ ЗАМОРАЖИВАТЬ.
Не смешивать Adcetris с или управлять как вливания с другими лекарственными продуктами.
Лекарственные формы и сильные стороны
Adcetris (brentuximab vedotin) для инъекций одноразового vial содержащих 50 мг brentuximab vedotin как стерильные, белый кремовый торт флаконов, консервант или порошка.
Периферийная невропатия
Лечение Adcetris вызывает периферической невропатии, преимущественно сенсорных. Периферийная невропатия Мотор также были случаи. Adcetris индуцированных периферической невропатии является совокупным. В HL и sALCL клинических испытаний 54% из пациентов пережили любого класса невропатии. Из этих пациентов 49% полной резолюцией, 31% имели частичное улучшение, а 20% не улучшилось. Пациентов, которые сообщили невропатии 51% имели остаточных невропатия во время их последней оценки. Мониторинг пациентов для симптомов невропатии, такие, как hypoesthesia, Гиперестезия, парестезию, дискомфорт, жжение, нейропатической боли или слабости. Пациенты испытывают новые или обострение периферийная невропатия может потребоваться задержка, изменения в дозы или прекращение Adcetris [см. Доза модификация (2.2) ].
Инфузионные реакции
Связанные с инфузия реакций, включая анафилаксии, имели место с Adcetris. Монитор пациента во время вливания. Если анафилаксии, немедленно и окончательно прекратить администрации Adcetris и администрировать соответствующей медицинской терапии. Если связанные с вливание происходит, настой должно быть прерван и соответствующие медицинские управления возбуждено. Пациенты, которые испытали ранее проблематике инфузии реакции следует premedicated для последующего настоев. Премедикация может включать ацетаминофен, антигистамин и кортикостероидами.
Полная крови счетчики должны контролироваться до каждой дозы Adcetris и более частого контроля следует рассматривать для пациентов с класса 3 или 4 нейтропения. Продлен тяжелой нейтропения (?1 неделя) может происходить с Adcetris. Если класс 3 или 4 нейтропения развивается, управлять, доза задержек, сокращений или сокращаемых [см. (Изменения) доза 2.2) ].
Синдром лизис опухолей
Синдром лизис опухолей может возникнуть. У больных с быстро многочисленных опухоли и бремя высоких опухоль может быть повышенного риска синдрома лизис опухолей. Тщательно контролировать и принимать соответствующие меры.
Синдром Стивенса - Джонсона
Синдром Стивенса - Джонсона было сообщено с Adcetris. Если возникает синдром Стивенса - Джонсона, прекратить Adcetris и администрировать соответствующей медицинской терапии.
Прогрессивные мультифокальном Leukoencephalopathy
Смертельный случай прогрессивного мультифокальном leukoencephalopathy (PML) зарегистрирован в пациента, который получил 4 химиотерапевтических препаратов до получения Adcetris.
Использование во время беременности
Существует не адекватных и контролируемых исследований Adcetris у беременных женщин. Однако основываясь на ее механизма действий и выводов в животных, Adcetris может повредить плода когда беременной женщине. Brentuximab vedotin причиной эмбриона и плода токсичность, включая значительное снижение эмбриона жизнеспособность и пороки развития плода, в животных в материнской воздействия, которые были аналогичны человеческого воздействия в рекомендуемых дозах для пациентов с HL и sALCL. Если этот препарат используется во время беременности или при получении препарата пациент становится беременной, пациент должен быть ознакомлены потенциальную опасность для плода [см. Использование в конкретных групп населения ( 8.1 ) ].
Клинический опыт судебного разбирательства
Потому что клинические испытания проводятся в разных условиях, неблагоприятные реакции тарифы в клинических испытаниях препарата нельзя сравнивать непосредственно к ставкам в клинических испытаниях другого наркотиков и могут не отражать ставки, на практике.
Adcetris изучался как монотерапии в 160 пациентов в два этапа 2 процесса. В обоих исследованиях наиболее распространенных побочных реакциях (?20%), независимо от причинности, были нейтропения, периферическая невропатия сенсорных, усталость, тошнота, анемия, инфекции верхних дыхательных путей, диарея, пирексия, сыпь, тромбоцитопения, кашля и рвота. Наиболее распространенными неблагоприятных реакций, происходящих в по меньшей мере 10% пациентов в любом испытании, независимо от причинности, используя NCI общей токсичности критерии версии 3.0, показаны в Таблица 1 .
Опыт работы в лимфомы Ходжкина
Adcetris был изучен в 102 больных с HL в одну руку, клинических испытаний в котором Рекомендуемая начальной дозы и расписание было 1,8 мг/кг внутривенно каждые 3 недели. Средняя продолжительность лечения было 27 недель (диапазон, 3-56 недель) [см. Клинические исследования (14) ].
Наиболее распространенных побочных реакциях (?20%), независимо от причинности, были нейтропения, периферическая невропатия сенсорных, усталость, инфекции верхних дыхательных путей, тошнота, диарея, анемия, пирексия, тромбоцитопения, сыпь, брюшной болью, кашель и рвота.
Опыт в области системного анапластические большой клеточная лимфома
Adcetris был изучен в 58 больных с sALCL в одну руку, клинических испытаний в котором Рекомендуемая начальной дозы и расписание было 1,8 мг/кг внутривенно каждые 3 недели. Средняя продолжительность лечения был 24 недель (диапазон, 3-56 недель) [см. Клинические исследования (14) ].
Наиболее распространенных побочных реакциях (?20%), независимо от причинности, были нейтропения, анемия, периферическая невропатия сенсорных, усталость, тошнота, пирексия, сыпь, понос и боли.
Комбинированные опыт
Таблица 1. Чаще всего сообщается О (?10%) Побочные реакции
*
От значения лабораторных и негативную реакцию данных
HL sALCL
Общая N = 102
% больных Общая N = 58
% больных
Неблагоприятные реакции Любое
Класс Класс
3 Класс
4 Любое
Класс Класс
3 Класс
4
Крови и лимфатической системы
Нейтропения * 54 15 6 55 12 9
Анемия * 33 8 2 52 2 -
Тромбоцитопения * 28 7 2 16 5 5
Лимфаденопатия 11 - - 10 - -
Заболевания нервной системы
Периферийная невропатия сенсорные 52 8 - 53 10 -
Периферийная невропатия Мотор 16 4 - 7 3 -
Головная боль 19 - - 16 2 -
Головокружение 11 - - 16 - -
Общие заболевания и условия сайта администрирования
Усталость 49 3 - 41 2 2
Пирексия 29 2 - 38 2 -
Озноб 13 - - 12 - -
Боль 7 - - 28 - 5
Отек периферийных устройств 4 - - 16 - -
Инфекции и вредителей
Инфекции верхних дыхательных путей 47 - - 12 - -
Желудочно-кишечные заболевания
Тошнота 42 - - 38 2 -
Диарея 36 1 - 29 3 -
Боли в области живота 25 2 1 9 2 -
Рвота 22 - - 17 3 -
Запор 16 - - 19 2 -
Кожи и подкожной ткани расстройств
Сыпь 27 - - 31 - -
Зуд 17 - - 19 - -
Алопеция 13 - - 14 - -
Ночное потение 12 - - 9 - -
Сухая кожа 4 - - 10 - -
Нарушения дыхания, грудной и средостения
Кашель 25 - - 17 - -
Одышка 13 1 - 19 2 -
Орофарингеального боли 11 - - 9 - -
Musculoskeletal и заболевания соединительной ткани
Артралгии 19 - - 9 - -
Миалгию 17 - - 16 2 -
Боли в спине 14 - - 10 2 -
Боль в верхней его части 10 - - 10 2 2
Мышечные спазмы 9 - - 10 2 -
Психические расстройства
Бессонница 14 - - 16 - -
Тревога 11 2 - 7 - -
Метаболизм и расстройства питания
Снижение аппетита 11 - - 16 2 -
Исследования
Вес снизился 6 - - 12 3 -
Инфузионные реакции
Два случая анафилаксия сообщалось в первый этап судебных разбирательств. Существует не класса 3 или 4 проблематике инфузии реакции в рамках этапа 2 исследований, однако сообщила о, 1 класса 2 реакций, связанных с инфузия сообщалось или 19 пациентов (12%). Наиболее распространенными побочными реакциями (?2%), связанные с инфузия реакций были озноб (4%), тошнота (3%), диспноэ (3%), зуд (3%), пирексия (2%) и кашель (2%).
Серьезных побочных проявлений
В рамках этапа 2 исследований тяжелых побочных реакциях, независимо от причинности, сообщалось в 31% пациентов, получавших Adcetris. Наиболее распространенных тяжелых побочных реакциях, испытываемых больных с HL включать Мотор периферической невропатии (4%), боли в животе (3%), легочная эмболия (2%), пневмониту (2%), пневмоторакса (2%), пиелонефрита (2%) и пирексия (2%). Наиболее распространенных тяжелых побочных реакциях, испытываемых у больных с sALCL, Септический шок (3%), суправентрикулярной аритмии (3%), боль в верхней его части (3%) и мочевыводящих путей инфекции (3%). Другие важные тяжелых побочных реакциях сообщили включены один случай каждый ПМЛ, синдром Стивенса - Джонсона и опухоли лизис синдрома.
Доза модификации
Неблагоприятные реакции, которая привела к доза задержек в более чем 5% пациентов были нейтропения (14%) и сенсорных периферической невропатии (11%) [см. (Изменения) доза 2.2) ].
Побочные реакции привели к прекращения лечения в 21% больных. Неблагоприятных реакций, которые привели к прекращения лечения в 2 или более больных с HL или sALCL были сенсорных периферической невропатии (8%) и мотор периферической невропатии (3%).
У больных с HL и sALCL в рамках этапа 2 исследований [см. Клинические исследования (14,1) ] прошли тест на антитела к brentuximab vedotin каждые 3 недели с помощью чувствительных electrochemiluminescent иммуноанализа. Примерно 7% пациентов в рамках этих исследований разработаны неизменно положительные антител (положительный тест на более чем 2 timepoints) и 30% разработали транзиторно позитивные антител (положительных в 1 или 2 post-baseline timepoints). Анти brentuximab антитела были направлены против антитела компонент brentuximab vedotin у всех больных с проездом или постоянно позитивные антител. Два из больных (1%) с опытным побочных реакциях неизменно положительные антител в соответствии с настой реакции, которая привела к прекращение лечения. В целом высокий уровень притока связанных реакция наблюдалась у больных, которых неизменно положительные антител.
В общей сложности 58 пациента образцы, которые были либо преходящий или постоянно позитивным для анти brentuximab vedotin антитела были протестированы на наличие нейтрализующих антител. Шестьдесят два процента этих пациентов имели по крайней мере один образец, который был положительным для присутствия нейтрализующих антител. Эффект анти brentuximab vedotin антител на безопасность и эффективность не известна.
Результаты анализа иммуногенности сильно зависит от нескольких факторов, включая пробирного чувствительность и специфичность, чт? методологии, пробами, времени сбора проб, сопутствующих препаратов и лежит в основе болезни. По этим причинам сравнение количество антител к Adcetris с уровнем антител к другие товары могут вводить в заблуждение.
Наркотиков взаимодействий
В пробирке данные указывают что монометиловый auristatin Е (MMAE). субстрат и ингибитор CYP3A4/5.
Влияние других препаратов на Adcetris
Ингибиторы CYP3A4/индукторов: MMAE прежде всего метаболизируются CYP3A [см. Клиническая фармакология) 12.3) ]. Совместное управление Adcetris с Кетоконазол, мощным CYP3A4 ингибитора, увеличение подверженности MMAE примерно 34%. Пациенты, которые получают сильное CYP3A4 ингибиторы одновременно с Adcetris следует тщательно контролировать для побочных реакций. Совместное управление Adcetris с rifampin, метаболизирующих CYP3A4, уменьшить воздействие MMAE примерно на 46%.
Влияние Adcetris на другие препараты
Совместное управление Adcetris не затрагивает подверженности мидазолам, CYP3A4 субстрата. MMAE не помешает другим CYP ферменты в соответствующих клинических концентрациях [см. Клиническая фармакология (12,3) ]. Ожидается, что Adcetris не изменить воздействие лекарств, которые метаболизируются CYP3A4 ферменты.
ИСПОЛЬЗОВАНИЕ В КОНКРЕТНЫХ ГРУППАХ НАСЕЛЕНИЯ
Беременность категории D [см. И предупреждения (5,7) ].
Существует не адекватных и контролируемых исследований с Adcetris у беременных женщин. Однако основываясь на ее механизма действий и выводов в животных, Adcetris может повредить плода когда беременной женщине. Brentuximab vedotin причиной эмбриона и плода токсичность в животных в материнской воздействия, которые были аналогичны человеческого воздействия в рекомендуемых дозах для пациентов с HL и sALCL. Если этот препарат используется во время беременности, или если пациент становится беременной при получении этот препарат, пациент должен быть ознакомлены потенциальную опасность для плода.
В эмбрион плода развития исследования крыс получил 2 внутривенного введения доз vedotin brentuximab 0.3, 1, 3 или 10 мг/кг в период organogenesis (один раз каждый на 6 дней беременности) и 13. Наркотиков индуцированных эмбриона и плода токсичность рассматривались главным образом в животных с 3 и 10 мг/кг наркотиков и включает более ранних рассасывания (?99%), post-implantation потери (?99%), уменьшилось количество живого плода и внешние пороки развития (то есть, пуповины грыжи и malrotated частей). Системное воздействие в животных в brentuximab vedotin дозе 3 мг/кг является примерно же воздействие в пациентах с HL или sALCL, которые получили Рекомендуемая доза/1,8 мг/кг каждые три недели.
Кормящих матерей
Не известно, ли brentuximab vedotin из организма в материнском молоке. Потому что многие препараты являются из организма в материнском молоке и из-за возможности для тяжелых побочных реакциях в грудных от Adcetris, следует принять решение, следует ли прекратить медсестер или прекратить наркотиков, принимая во внимание значение препарата с матерью.
Детская использования
Безопасность и эффективность Adcetris не были созданы в педиатрической популяции. Клинические испытания Adcetris включены только 9 педиатрических больных, и это число не достаточно, чтобы определить ли они реагируют иначе, чем взрослых пациентов.
Гериатрические использования
Достаточное количество пациентов в возрасте 65 лет и над определить ли они реагируют по-разному от более молодых пациентов не включали клинические испытания Adcetris. Безопасность и эффективность не была учреждена.
Почечная обесценение
Почки является маршрут экскреции для MMAE. Не было определено влияние почек обесценения на фармакокинетики MMAE.
Печеночных обесценение
Печень является маршрут очистки для MMAE. Не было определено влияние печеночных обесценения на фармакокинетики MMAE.
Нет никаких известных противоядием для overdosage Adcetris. В случае overdosage, пациент должен внимательно следить за неблагоприятных реакций, особенно нейтропения, и благоприятной лечение должно быть назначено.
Adcetris описание
Adcetris (brentuximab vedotin) является направлены CD30 антител наркотиков конъюгированная (АЦП), состоящая из трех компонентов: 1 плоидности IgG1 антитела cAC10, специфические для человеческого CD30, 2) микротрубочек совершалась агент MMAE и 3) протеазы отщепляемого компоновщик covalently придает MMAE cAC10.
Brentuximab vedotin имеет приблизительный молекулярный вес 153 кДа. Примерно 4 молекул MMAE прикреплены к каждому молекулы антител. Brentuximab vedotin получается путем химических сопряжение антитела и малые молекулы компонентов. Антитела производится на клетки млекопитающих (китайского хомяка яичник), и небольшие молекулы компоненты производятся путем химического синтеза.
Adcetris (brentuximab vedotin) для инъекций поставляется стерильной, белый кремовый, консервант лиофилизированным торт или порошка в одноразовых флаконов. После воссоздания 10.5 мл с производится стерильная вода для инъекций, USP, решение с 5 мг/мл brentuximab vedotin. Восстановленный продукт содержит дигидрата Трегалоза 70 мг/мл, цитрат натрия дигидрата 5,6 мг/мл, лимонная кислота моногидрат 0,21 мг/мл и 0.20 мг/мл polysorbate 80 и вода для инъекций. PH-примерно 6,6.
Adcetris - клиническая фармакология
Механизм действия
Brentuximab vedotin является ADC. Антитело является нереальным IgG1, направленные против CD30. Малые молекулы, MMAE, является микротрубочек, нарушая агента. MMAE covalently прилагается к антителу через компоновщика. Nonclinical данные указывают на то, что противораковых деятельность Adcetris-за связывание АЦП для выражения CD30 клеток, а затем интернализации ADC?CD30 комплекса и выпуск MMAE через протеолитических расщепления. Связывание MMAE тубулина нарушает сети микротрубочек внутри клетки, впоследствии вызвать смерть клеточного цикла арест и apoptotic клеток.
Фармакодинамики
Потенциал пролонгации QT/QTc
Эффект brentuximab vedotin (1,8 мг/кг) на QTc интервале оценивалась в открытое этикетки, сингл АРМ исследования в 46 анализу больных с выражением CD30 гематологические злокачественных опухолей. Администрация brentuximab vedotin не затягивать средняя QTc интервал > 10 мс от базовой линии. Небольшое увеличение в среднем интервале QTc (